
Sociedad Chilena de Endocrinología Ginecológica
POSTURA DE SOCHEG
FRENTE A ARTÍCULO DE FITZPATRICK Y BERAL SOBRE ASOCIACIÓN DE RIESGO DE CÁNCER DE MAMA Y ANTICONCEPCIÓN HORMONAL
COMUNICADO SOBRE RIESGO DE CANCER DE MAMA ASOCIADO AL USO DE ANTICONCEPTIVOS HORMONALES
A raíz de la publicación reciente en un portal de noticias nacional titulada “Todos los anticonceptivos hormonales aumentan el riesgo de cáncer de mama”, creemos importante tranquilizar tanto a los profesionales de la salud como a las usuarias con relación a este tema.
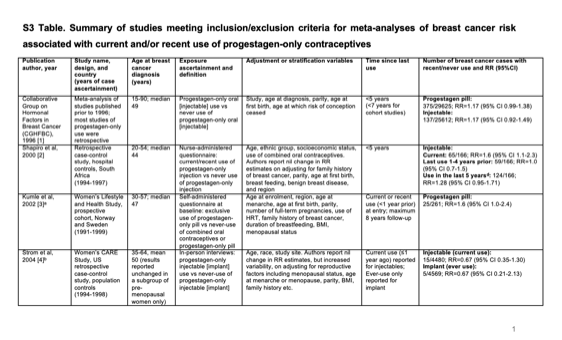
El estudio titulado “Combined and progestagen-only hormonal contraceptives and breast cancer risk: a UK nested case- control study and meta-analysis,” fue publicado por Fitzpatrick et al. en la revista Plos Medicine en marzo del presente año (PLoS Med 2023 20(3): e1004188)
Este es un estudio observacional que investiga la asociación entre usuarias actuales o recientes (últimos 10 años) de anticonceptivos hormonales con casos de cáncer de mama diagnosticados, con énfasis en los que contienen solo progestágenos (píldora, inyectable, implantes o dispositivos intrauterinos medicados con levonorgestrel).
Hay que aclarar que es un estudio de casos y controles, metodología que se sabe expuesta a múltiples sesgos de selección y otros sesgos incontrolables, especialmente en la conformación del grupo control, que es una población que se estima comparable o al menos con una condición de vida semejante. Normalmente no se realiza aleatorización de los sujetos de ambos grupos como es el caso de este estudio, el que solo compara usuarias con no usuarias en un determinado período de tiempo de observación y determinada edad (menores de 50 años), desconociéndose otras características relevantes al momento de evaluar probabilidad de riesgo con los datos observados. Peor aún, expresar resultados de asociación (odds ratio), en el mejor de los casos, expresa datos muy aproximados y su mayor valor consiste en destacar algún aspecto epidemiológico posible, en este caso desarrollar un cáncer de mama invasor, sin demostrar causalidad.Tampoco da información de mayor ocurrencia o incidencia de mortalidad para el grupo expuesto.
El informe también combina estos datos con análisis de estudios previos para intentar un metaanálisis, pero también en este cometido carece de las condiciones muestrales de homogeneidad y neutralidad en la selección de los estudios como para considerarlo como pieza importante de evidencia.
El estudio concluye que sus resultados serían concordantes con los hallazgos de estudios previos, también casos/controles y observacionales, en una selección de publicaciones que incluyen como referencia estudios previos propios, que se han caracterizado por tener sesgo ideológico tratando de asociar el uso de diversas hormonas con un supuesto aumento de casos de cáncer.
Inician su análisis con un estudio autorreferente del Collaborative Group on Hormonal Factors in Breast Cancer, que agrupa gran cantidad de pacientes tratadas con medroxiprogesterona en tratamientos de menopausia, cuando no se conocía el riesgo de ésta. Por esta razón, es que prácticamente está en desuso al menos en terapia hormonal de la menopausia (THM) y tiene detractores cuando es usada como AH y contraindicaciones precisas (categoría 3) en usuarias con riesgo cardiovascular con morbilidad múltiple como obesidad, tabaquismo, hipertensión arterial, por nombrar las más relevantes y comunes para la población de mujeres chilenas. El estudio no entrega estos datos y tampoco los criterios elegidos por los prescriptores en Reino Unido. Concluyen la existencia de asociación proveniente de algunos estudios con bajo poder estadístico, pero desestiman la ausencia de asociación del único estudio prospectivo aleatorizado, que no encuentra esa asociación (Dinger et al).
Cada vez existe mas prescripción de anticonceptivos hormonales que contienen solo progestágenos. La evidencia sobre su uso y el riesgo de cáncer de mama ha sido menos estudiada que para los métodos combinados. Es probable que el mayor uso de AH de sólo progestágenos incluya población de mayor riesgo conocido de desarrollar un cáncer de mama (obesidad) que puede en muchos casos no recomendar el uso de un AHC.
El estudio informa un aumento similar y significativo del riesgo de cáncer de mama en usuarias de anticonceptivos hormonales combinados (RR 1.23), píldoras de progestágenos solos (RR 1.26), progestágeno inyectable (RR 1.25) y usuarias de DIU liberadores de progestágeno (RR:1.32). El riesgo iría disminuyendo luego de la suspensión del método y desaparecería 10 años después.
El riesgo de cáncer de mama aumenta con la edad y es bajo en mujeres en edad reproductiva, por lo que es importante aclarar que un aumento del riesgo relativo de cáncer de mama de un 25% no significa un gran aumento del riesgo absoluto. Por esto, es más importante estimar el exceso de riesgo que confiere el uso de anticonceptivos hormonales. Así, suponiendo que los datos fueran certeros, luego de 5 años de uso de anticonceptivos hormonales combinados o de solo progestágeno, el aumento del riesgo absoluto para los siguientes 15 años podría llegar a 8 casos por 100.000 usuarias entre los 16 y los 20 años y a 265 casos por 100.000 usuarias entre los 35 y los 39 años.
A mayor edad de las usuarias, su riesgo basal de cáncer aumenta. Aun así, el aumento del riesgo asociado al uso de ACH es escaso. Si una mujer usa anticonceptivos hormonales entre los 25 y los 29 años, en los 15 años luego de la suspensión de su uso, su riesgo de cáncer de mama aumenta de 0.5 a 0.57%. Para mujeres usuarias entre 35 y los 39 años, el riesgo equivalente parece ser de 2% a 2.2%.
Vistos en perspectiva estos datos y considerando que diversas hormonas, de distinta naturaleza, algunas con mínima circulación, como los DIU-LNG, dan en este análisis riesgos similares, es legítimo preguntarse, cuál de los factores de ser usuaria de anticonceptivos hormonales o mejor dicho de un determinado AH es el que realmente podría asociarse a un aumento significativo de padecer de algún cáncer o simplemente de fallecer por esta eventual asociación.
Son numerosos los beneficios conocidos de los AHC, más allá del evidente beneficio de disminuir los embarazos no deseados. Es sabida la disminución que confieren del riesgo de cáncer de colon, endometrio y ovario en las usuarias, entre otros efectos beneficiosos no contraceptivos.
SOCHOG, SOCHEG, SOCHICLIM y SOGIA compartimos la recomendación de no cambiar la práctica actual de prescripción de anticonceptivos por esta nueva evidencia, pero invitamos a incluir esta información en la consejería individual que se debe realizar a las usuarias en relación a los riesgos y beneficios de los distintos métodos anticonceptivos actualmente disponibles, conscientes que la nueva información, al igual que otros estudios de asociación de riesgo, deja más interrogantes, que respuestas.
Bibliografía
1. Mørch LS Skovlund CW Hannaford PC Iversen L Fielding S Lidegaard Ø. Contemporary hormonal contraception and the risk of breast cancer. N Engl J Med. 2017; 377: 2228-2239
2. Hormonal contraception and risk of breast cancer and breast cancer in situ among Swedish women 15−34 years of age: A nationwide register-based study. The Lancet Regional Health – Europe 2022;21: 100470 Published online 29 July 2022 https://doi.org/10.1016/j.lanepe.2022.100470
3. Vinogradova Y Coupland C Hippisley-Cox J. Use of hormone replacement therapy and risk of breast cancer: nested case-control studies using the QResearch and CPRD databases. BMJ (Clin Res Ed). 2020; 371: m3873
4. Busund M Bugge NS Braaten T Waaseth M Rylander C Lund E. Progestin-only and combined oral contraceptives and receptor-defined premenopausal breast cancer risk: the Norwegian women and cancer study. Int J Cancer. 2018; 142: 2293-2302
5. Samson M Porter N Orekoya O et al. Progestin and breast cancer risk: a systematic review.
Breast Cancer Res Treat. 2016; 155: 3-12 6. Depot medroxyprogesterone acetate and breast cancer. A pooled analysis of the world health organization and New Zealand studies. JAMA. 1995; 273: 799-804
7. Strom BL Berlin JA Weber AL et al. Absence of an effect of injectable and implantable progestin-only contraceptives on subsequent risk of breast cancer. Contraception. 2004; 69: 353-360
8. Jareid M Thalabard JC Aarflot M Bøvelstad HM Lund E Braaten T. Levonorgestrel-releasing intrauterine system use is associated with a decreased risk of ovarian and endometrial cancer, without increased risk of breast cancer. Results from the NOWAC Study. Gynecol Oncol. 2018; 149: 127-132
9. Oral contraceptive use and breast cancer risk according to molecular subtypes status: a systematic review and meta-analysis of case-control studies. Cancers (Basel). 2022; 14574
10. Conz L Mota BS Bahamondes L et al. Levonorgestrel-releasing intrauterine system and breast cancer risk: a systematic review and meta-analysis. Acta Obstet Gynecol Scand. 2020; 99:970-982
Nuestra sociedad realizó un trabajo conjunto con SOCHOG de análisis de la reciente publicación de Fitzpatrick que onforma asociación entre riesgo de cáncer de mama y anticonceptivos hormonales, basados en un estudio anidado de casos y controles en la base de datos del UKPDS. Este análsis ha sido acogido y suscrito también por SOGIA y SOCHICLIM.


Artículo original de Fitzpatrick et al
DESCARGAR PDF


Declaración conjuta SOCHOG, SOCHEG, SOGIA, SOCHICLIM
ABRIR PDF DECLARACION CONJUNTA